腹 膜 假 性 黏 液 瘤 互 助 联 盟
China Pseudomyxoma Peritonei (PMP) Patient Support Group

自助 助人 温暖 希望
本文收录: 许洪斌,蔡莺. 腹膜假黏液瘤典型病案分析[M]. 2021年11月 第一版.北京:科学出版社, 2021:9—13
细胞减灭术加腹腔热灌注化疗是治疗腹膜转移肿瘤,特别是腹膜假黏液瘤的规范治疗 方式[1-4] ,但在应用之初,此治疗方式在世界各地发展程度不一,直至2014年在荷兰阿姆 斯特丹召开的第九届国际腹膜癌大会上,才正式提出了《肿瘤细胞减灭术加腹腔热灌注化 疗的国际建议》[International Recommendations for Cytoreductive Surgery ( CRS) and Hyperthermic Intraperitoneal Chemotherapy ( HIPEC)],这才确立了 CRS+HIPEC 在腹膜假黏液瘤治疗中的地位。国内腹膜癌领域专家于2015年联合发表了《细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识》,以下内容摘录及参考于此共识。
(一) 细胞减灭术方案
CRS包括脏器切除和腹膜切除,力争能够完全切除腹盆腔内肉眼可见的肿瘤。切除步骤包括全腹膜切除、左上腹膜切除、大网膜切除加脾切除、右上腹膜切除、盆腔腹膜切除加直肠乙状结肠切除、胆囊切除加小网膜切除及网膜囊剥除,可能还需要进行右半结肠切除或全结肠切除。手术之前可借助辅助检查初步制订CRS的范围。根据2015 版《细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识》:通过完善的术前影像学检查有助于对患者进行筛选,制订CRS方案。术前影像学检查包括静态影像学检查和动态影像学检查两部分:①在静态影像学检查方面,腹盆腔多层螺旋CT增强扫描+多平面重建对诊断腹膜癌(peritoneal carcinomatosis, PC )总体敏感度78.1%,特异度为92.3%;病灶长径≥12.5px时,敏感度为90.0%;病灶长径< 12.5px时,敏感度为 42.6% 。CT腹膜癌指数与术中PCI的吻合度为0.384~0.640[5] 。PC的典型CT表现包括腹膜呈条状增厚强化;大网膜结节状、条状、云絮状增厚并强化;肠管不对称性增厚或不规则狭窄并强化;小肠系膜呈结节状、“椒盐”征增厚并强化;腹腔及肠间隙积液。结合典型表现、病灶大小,可估算术前CT-PCI评分,用于判断患者PC播散程度。除了常规 CT检查外,还可以考虑进行PET/CT检查。②在动态影像学检查方面,可行胃肠道动态造影检查,观察肠管蠕动、分布状况及对比剂通过各段小肠时间,判断胃肠动力、肠管是否梗阻及肠系膜挛缩情况。以下3种影像学特点提示难以达到完全肿瘤细胞减灭:①小肠节段性梗阻;②肿瘤与小肠及系膜交互存在;③小肠表面或系膜可见长径>125px的肿瘤结节。此时应慎重选择HIPEC,必要时行腹腔镜探查,进行PCI评分,预估是否可达到 CCR-0~CCR-1切除,然后再决定是否进行CRS+HIPEC[6]。
术前评估适合采用CRS+HIPEC治疗患者的具体手术方式:取剑突至耻骨联合的长正中切口,充分显露术野,通常的操作顺序为肝圆韧带、大网膜、小网膜、右上腹、左上腹、膈面腹膜、侧壁腹膜、右器髂窝、左髂窝、盆底腹膜和小肠系膜,行最大程度CRS,对壁腹膜进行区域性整片剥脱术,对脏腹膜和肠道器官采用病变肠管切除术,对易形成肿瘤种植的胆囊窝、脾窝、道格拉斯腔,可切除胆囊、脾、直肠及子宫附件。肿瘤与重要器官粘连而不能切除者,可用球形电刀气化、炭化肿瘤组织,然后进行细胞减灭程度评分[6]。
(二)细胞减灭程度
细胞减灭程度(completeness of cytoreduction, CCR )是评估CRS手术程度的指标, 其与生存期密切相关,临床上常用的是Sugarbaker CCR评分法[7]。0分:CRS后术野无肉 眼可见肿瘤;1分:残余瘤直径<2.5mm; 2分:残余瘤直径2.5mm~62.5px; 3分:残余瘤直径>62.5px,或腹盆腔内存在无法切除病灶。以残余瘤直径不超过2.5mm( 0分和1分)被视为彻底的CRS。
(三)腹膜癌指数
规范的手术记录通常要对术中肿瘤负荷进行标准化评估。Sugarbaker腹膜癌指数 (peritoneal carcinomatosis index, PCI)评分是最常用的腹膜癌分期系统[7]。该法将腹部分成13个区,其中,0代表此区域未发现种植病灶;“1”代表此区域最大种植病灶直径< 12.5px;“2”代表此区域最大种植病灶直径为0.5~125px; “3”代表最大种植病灶直径>125px。每个区的肿瘤负荷评分总和就是PCI评分(图3-1 )。PCI评分非常重要,有助于选择合适的治疗。
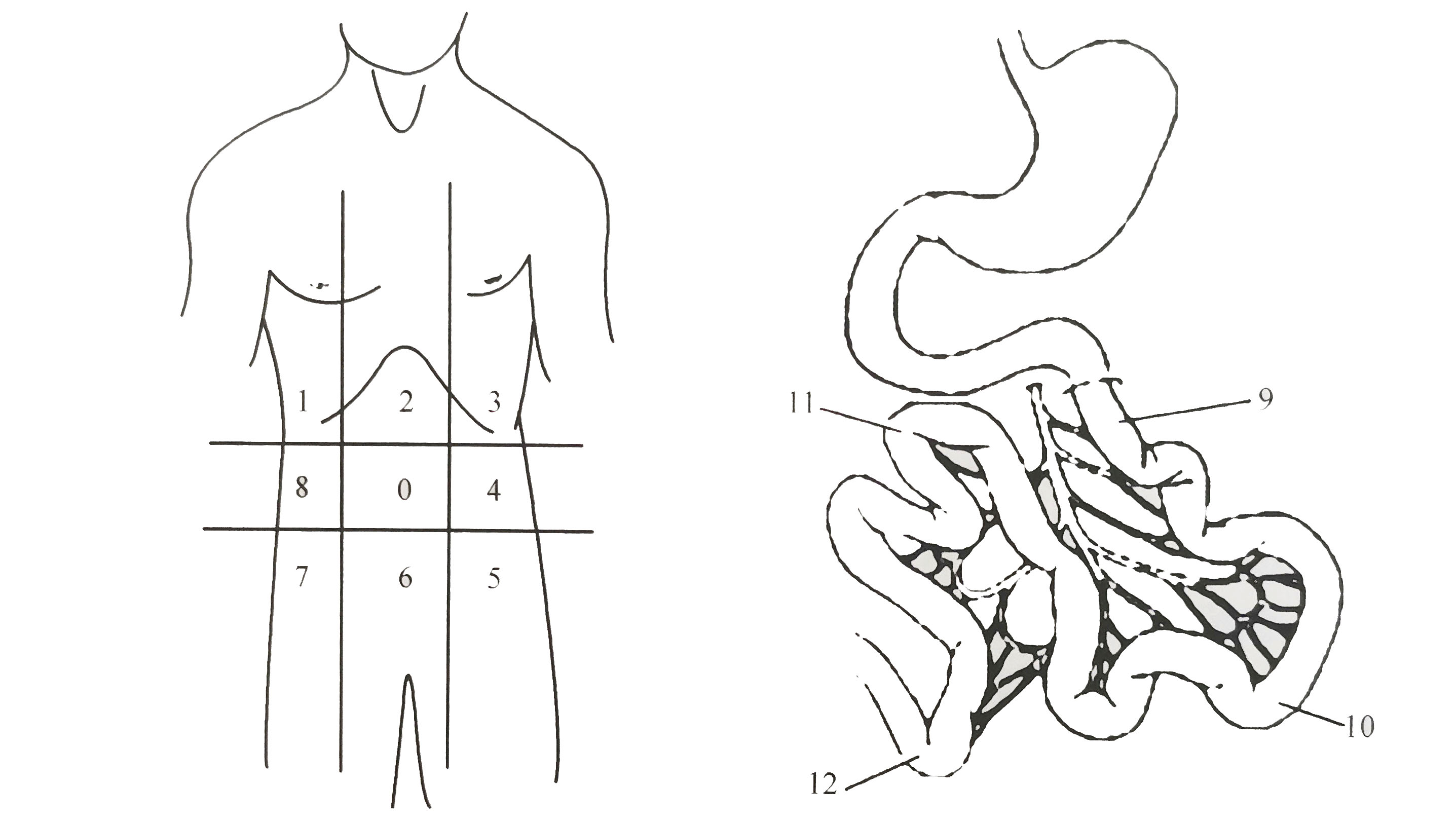
图3-1 PCI评分中应用的腹部13分区法
0.中腹部;1.右季肋部;2.上腹部;3.左季肋部;4.左腰部;5.左髂部;6.下腹部;7.右髂部;8.右腰部;9.空肠上段;10.空肠下段;11.回肠上段;12.回肠下段
根据2015版《细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识》:腹膜假黏液瘤是CRS+HIPEC的最佳适应证。有4项研究评估了CRS+HIPEC治疗腹膜假黏液瘤的疗效,5年生存率为66%~97%,不良事件发生率为27%~44%,死亡率为2.7%~13%[8-10]。法国进行的一项多中心临床研究[11],共301例腹膜假黏液瘤患者接受该疗法,5年生存率为73%,无病生存率为56%。CRS+HIPEC已成为腹膜假黏液瘤首选治疗方案。
(四) CRS 与 HIPEC
对于腹膜肿瘤患者,在行HIPEC前应尽可能实施CRS,以最大限度地清除肉眼可见肿瘤,为HIPEC提供良好的条件,而HIPEC可消除或缩小CRS术后残存的病灶。两者相辅相成,近年来在治疗腹膜恶性肿瘤上取得了很好的效果。对于经过CRS可以达到残余癌瘤直径<2.5mm的部分PC患者,即彻底的CRS手术后,联合HIPEC,有可能达到临床治愈。
(五) 单中心经验
笔者所在科自2006年开始收治腹膜假黏液瘤患者,并于2012年成立腹膜假黏液瘤治 疗中心,迄今已完成腹膜假黏液瘤相关CRS+HIPEC超过1000例次,相关数据资料正在收集整理(图3-2~图3-7)。
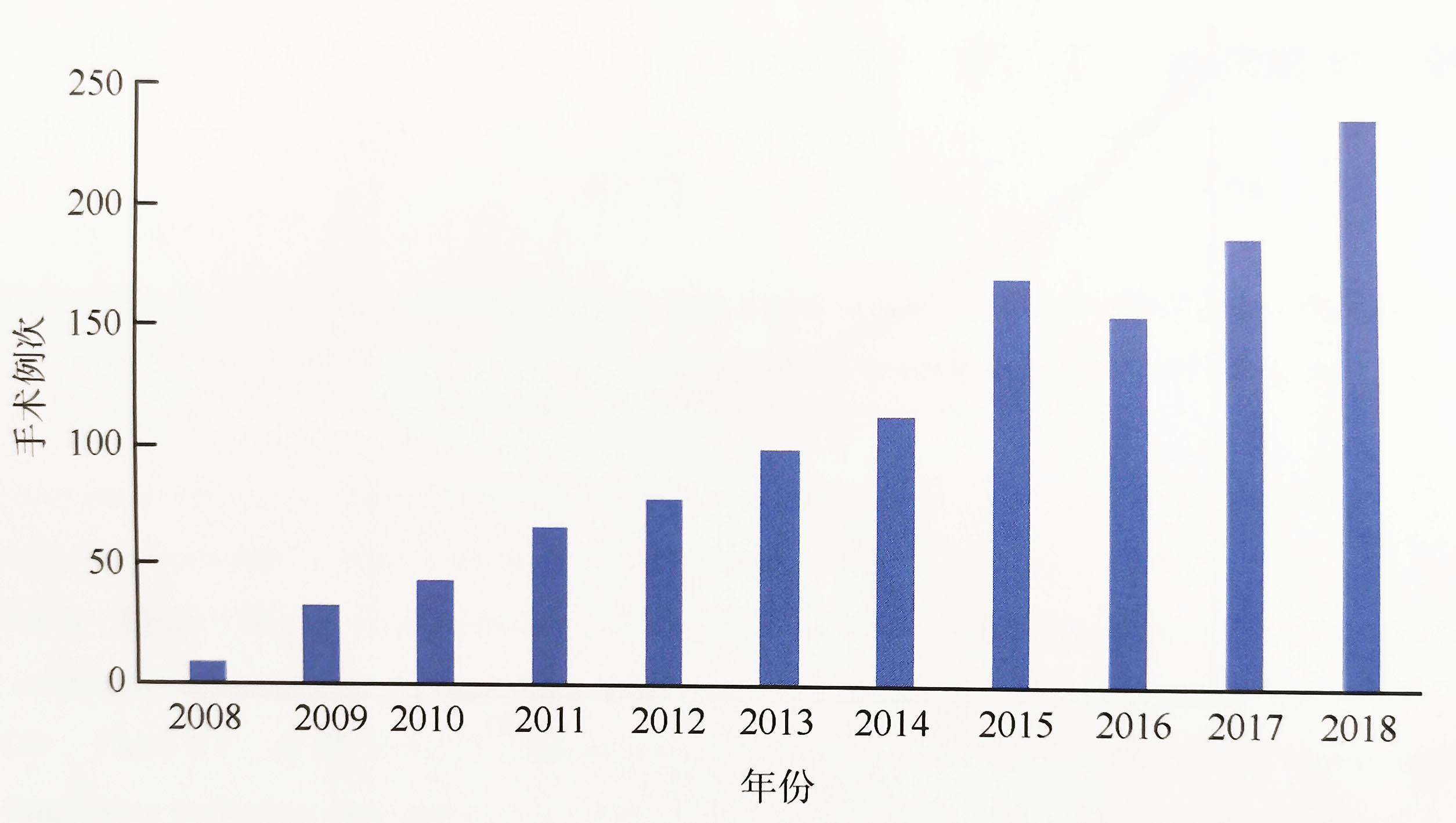 图3-2航天中心医院历年腹膜假黏液瘤手术例次
图3-2航天中心医院历年腹膜假黏液瘤手术例次
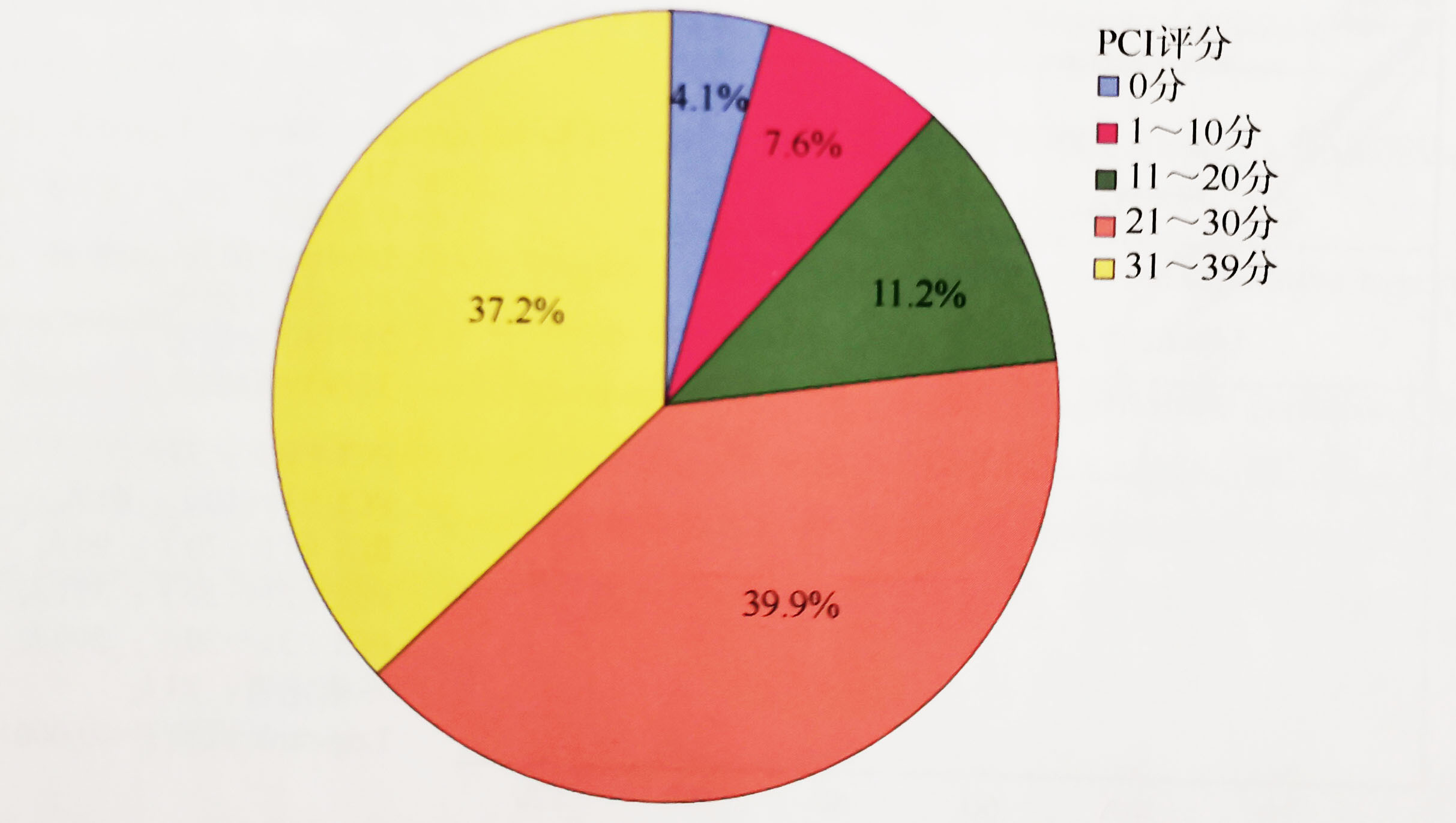 图3-3术中PCI评分情况:约77%的患者PCI评分> 20分
图3-3术中PCI评分情况:约77%的患者PCI评分> 20分
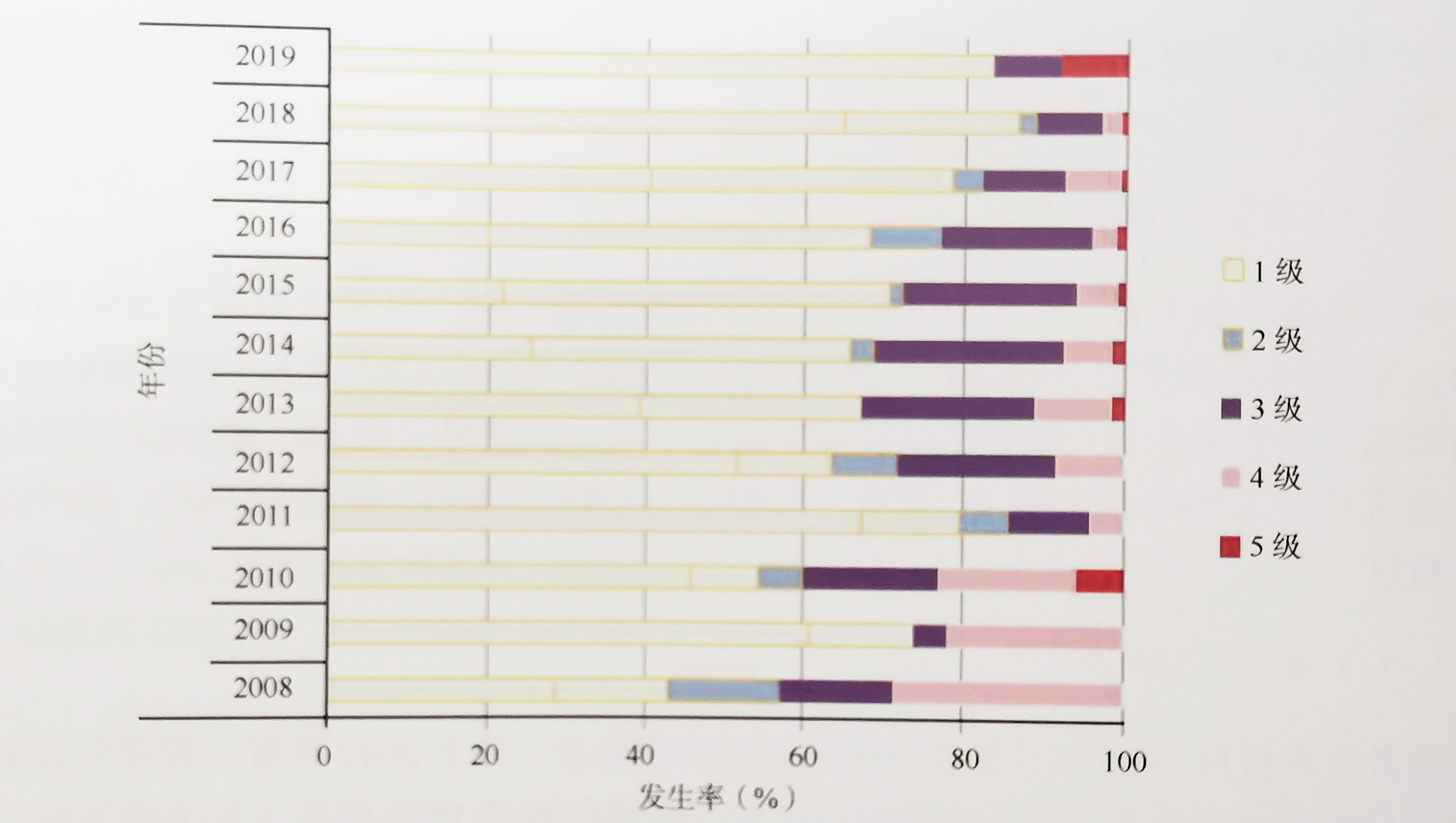 图3-4历年手术并发症发生情况:主要并发症(3级及以上)呈下降趋势
图3-4历年手术并发症发生情况:主要并发症(3级及以上)呈下降趋势
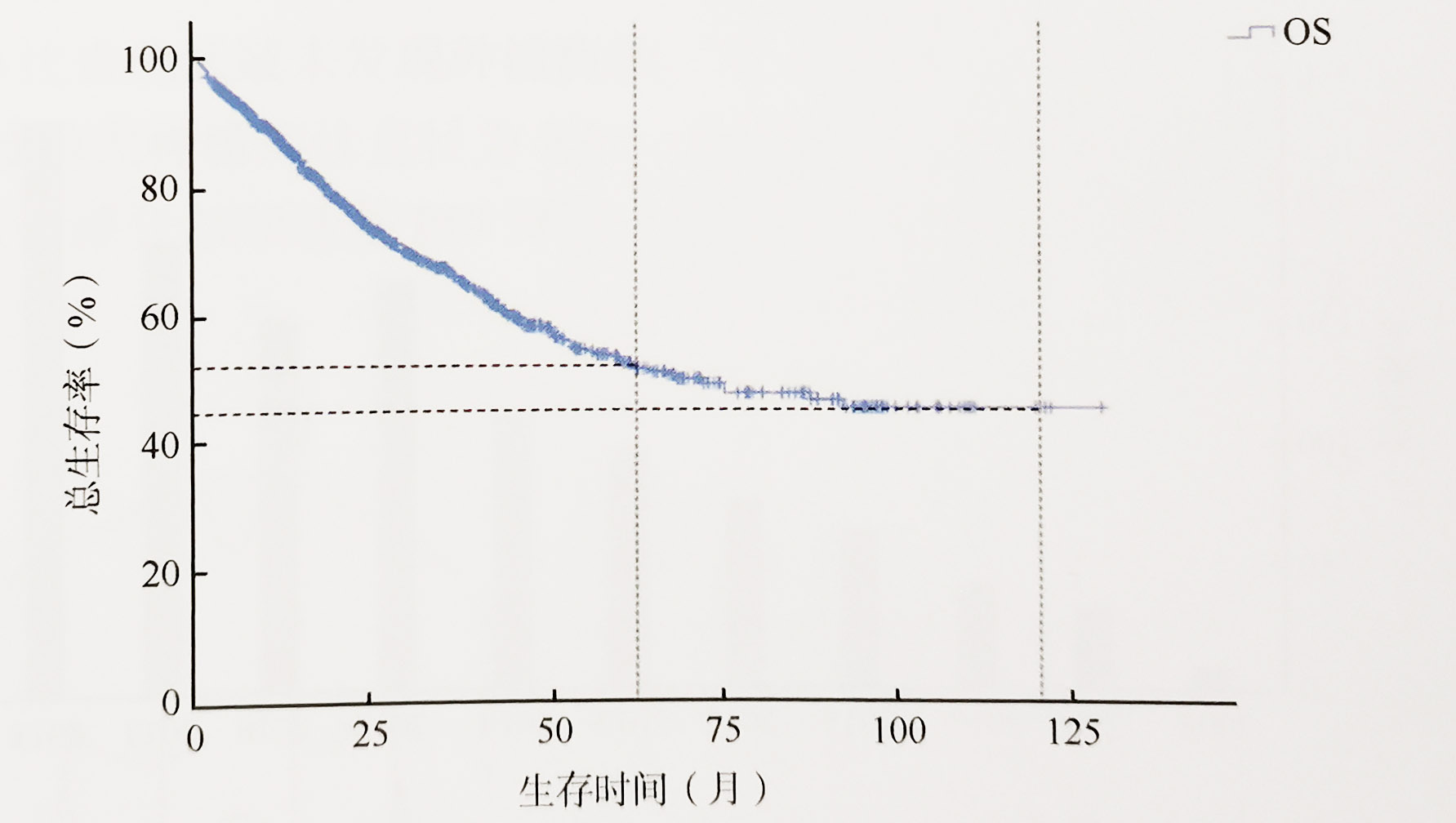 图3-5 K-M曲线
图3-5 K-M曲线
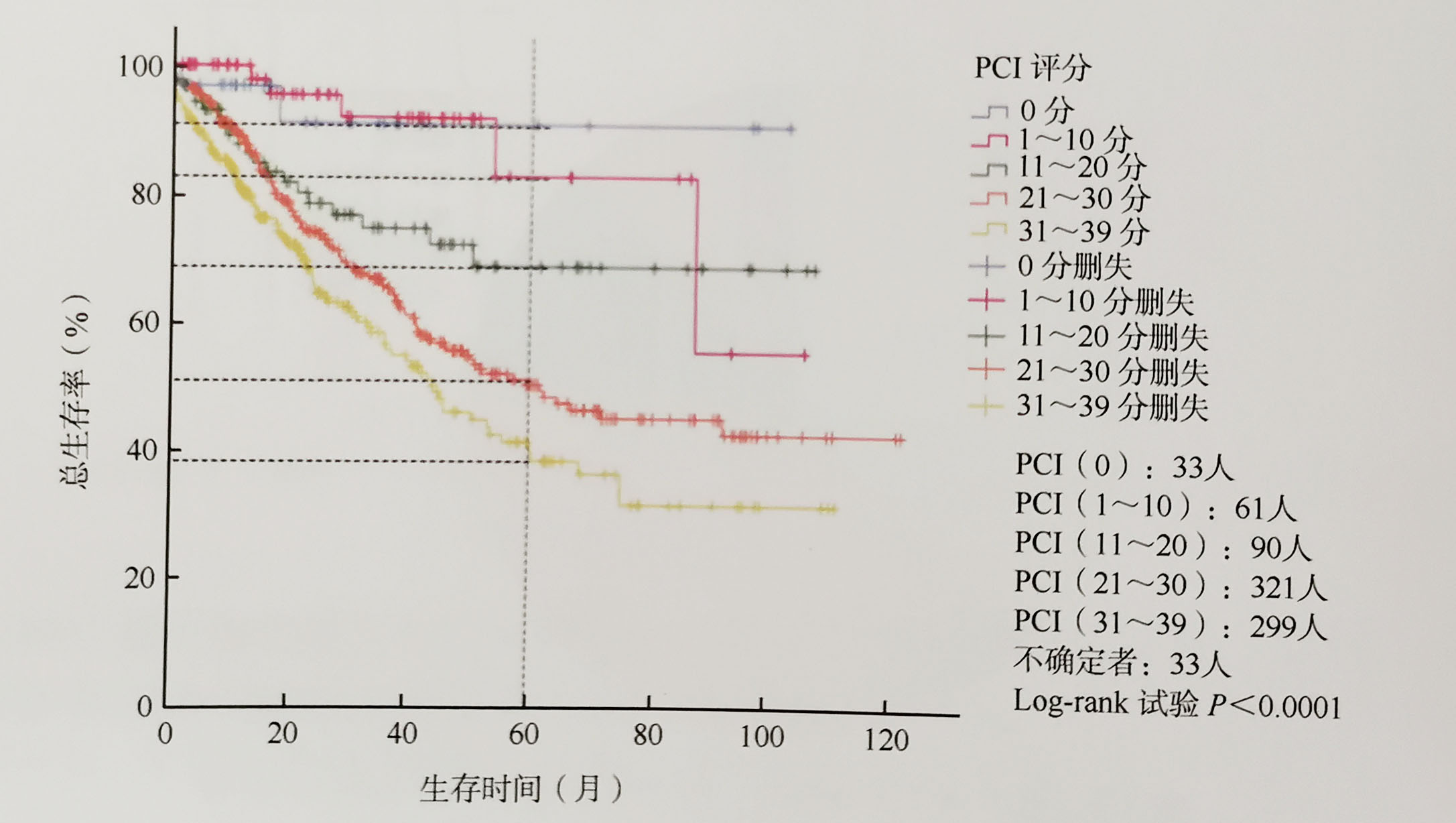 图3-6 PCI评分与预后显著相关(K-M曲线)
图3-6 PCI评分与预后显著相关(K-M曲线)
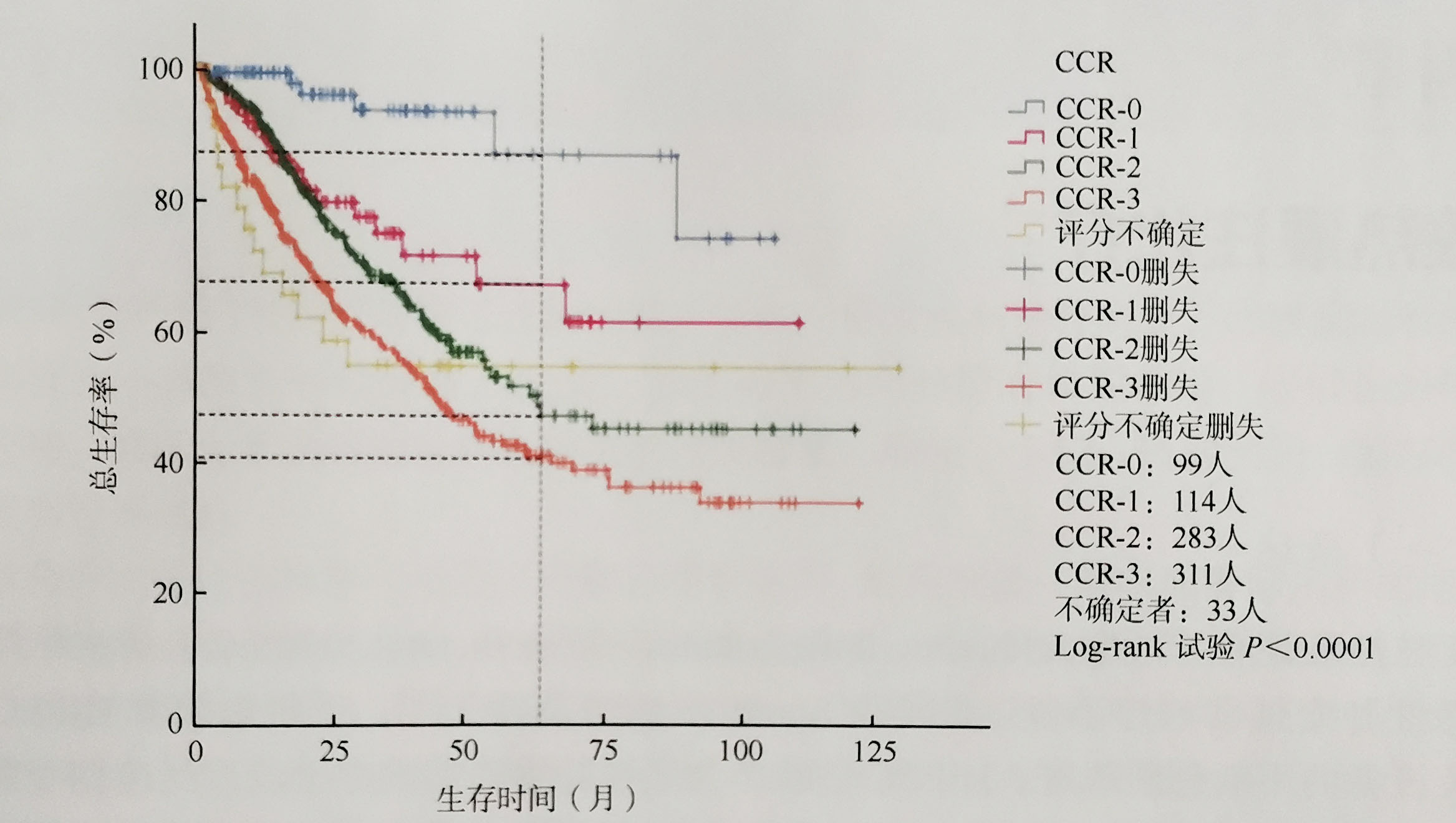 图3-7手术根治程度CCR与预后显著相关(K-M曲线)
图3-7手术根治程度CCR与预后显著相关(K-M曲线)
(撰稿:蔡莺,夏奥;校审:许洪斌)
参考文献
[1] Yang XJ, Huang CQ, Suo T, et al. Cytoreductive surgery and hyperthermic intra-peritoneal chemotherapy improves survival of patients with peritoneal carcinomatosis from gastric cancer: final results of a phase IQ randomized clinical trial. Ann Surg Oncol, 2011, 18 (6) : 1575-1581.
[2] Li Y. My standpoint of perioneal carcinomatosis study. Chin J Clin Oncol, 2012, 39 ( 22 ) : 1685-1686.
[3] Sticca RP. Peritoneal carcinomatosis: a final frontier. Ann Surg Oncol, 2003, 10 (5 ) : 484-485.
[4] Pilati P, Mocellin S, Rossi CR, et al. Cytoreductive surgery combined with hyperthermic intraperitoneal intraoperative chemotherapy for peritoneal carcinomatosis arising from colon adenocarcinoma. Ann Surg Oncol, 2003, 10 ( 5 ) : 508-513.
[5] Mei LJ, Wang LW, Zhou YF, et al. Role of contrast-enhanced multi-detector row computed tomography and multiplanar reconstruction in diagnosing peritoneal carcinomatosis. Chin J Clin Oncol, 2012, 39 (22) : 1745-1749.
[6] 李雁,周云峰,梁寒,等.细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识.中国肿瘤临床,2015, 42 (4): 198-205.
[7] Jacquet P, Sugarbaker PH. Clinical research methodologies in diagnosis and staging of patients with peritoneal carcinomatosis. Cancer Treat Res, 1996, 82: 359-374.
[8] Sugarbaker PH, Chang D. Results of treatment of 385 patients with peritoneal surface spread of appendiceal malignancy. Ann Surg Oncol, 1999, 6 (8): 727-731.[9] Witkamp AJ, de Bree E, Kaag MM, et al. Extensive surgical cytoreduction and intraoperative hyperthermic intraperitoneal chemotherapy in patients with pseudomyxoma peritonei. Br J Surg, 2001, 88 ( 3 ) : 458-463.
[10] Deraco M, Baratti D, Inglese MG, et al. Peritonectomy and intraperitoneal hyperthermic perfusion (IPHP) : a strategy that has confirmed its efficacy in patients with pseudomyxoma peritonei. Ann Surg Oncol, 2004, 11 (4 ) : 393-398.
[11] Elias D, Gilly F, Quenet F, et al. Pseudomyxoma peritonei: a French multi-centric study of 301 patients treated with cytoreductive surgery and intraperitoneal chemotherapy. Eur J Surg Oncol, 2010, 36 ( 5 ) : 456-462.
最新文章



